「ジアセントⓇ」殺菌性能試験および安定性試験結果
1.微酸性電解水「ジアセントⓇ」を用いた大腸菌・黄色ブドウ球菌・サルモネラ菌・腸炎ビブリオ菌・緑膿菌・セレウス菌の殺菌評価試験結果
2021年11月12日(株式会社信濃公害研究所)
1.目的
10の4~6乗オーダーの大腸菌・黄色ブドウ球菌・サルモネラ菌・腸炎ビブリオ菌・緑膿菌・セレウス菌(6菌種)に対する微酸性電解水「ジアセントⓇ」30ppmの殺菌力を調査する。
2.試験試料
- 大腸菌
- 黄色ブドウ球菌
- サルモネラ菌
- 腸炎ビブリオ菌
- 緑膿菌
- セレウス菌
- 微酸性電解水「ジアセントⓇ」(pH6.5 有効塩素量 29ppm)
3.試験方法
- 試験開始前に、大腸菌・黄色ブドウ球菌・サルモネラ菌・腸炎ビブリオ菌・緑膿菌・セレウス菌の菌株を用いて菌液を作成する。
- ブランクと微酸性電解水接触後の菌数について評価する。
- 微酸性電解水:8.9ml+供試菌液:1ml+チオ硫酸ナトリウム0.1ml、接触時間30秒(大腸菌・黄色ブドウ球菌・サルモネラ菌・腸炎ビブリオ菌・緑膿菌)、3分(セレウス菌)
- 試験は、それぞれの処理についてサンプル数を3検体で実施する。
- 培養条件
大腸菌・黄色ブドウ球菌・サルモネラ菌・緑膿菌・セレウス菌
| 培地 | 標準寒天培地 |
|---|---|
| 培養温度 | 36±1℃ |
| 培養時間 | 48時間 |
腸炎ビブリオ菌
| 培地 | 3%NaCl加標準寒天培地 |
|---|---|
| 培養温度 | 36±1℃ |
| 培養時間 | 48時間 |
4.試験結果
結果をまとめたものを表-1、図-1~6に示す。
表-1 試験結果一覧表







図-1 大腸菌殺菌試験
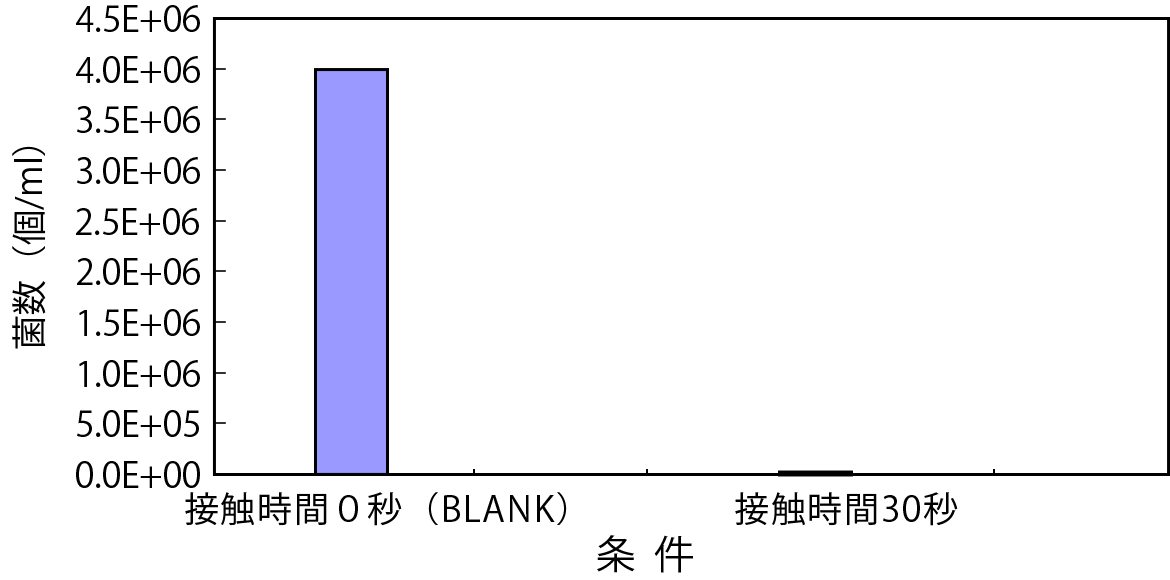
図-2 黄色ブドウ球菌殺菌試験

図-3 サルモネラ菌殺菌試験

図-4 腸炎ビブリオ菌殺菌試験
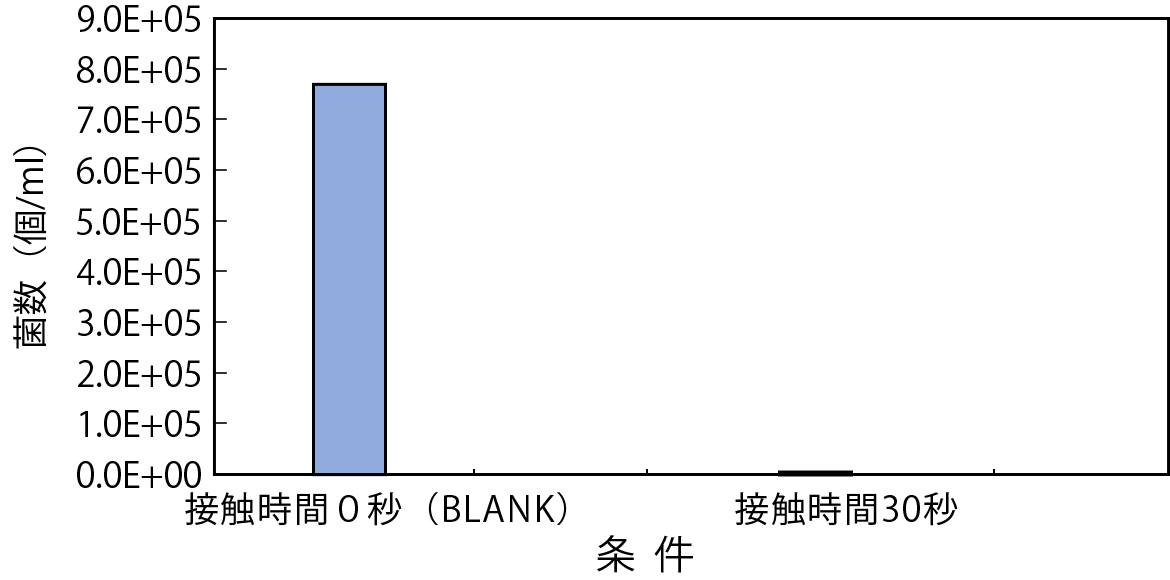
図-5 緑膿菌殺菌試験
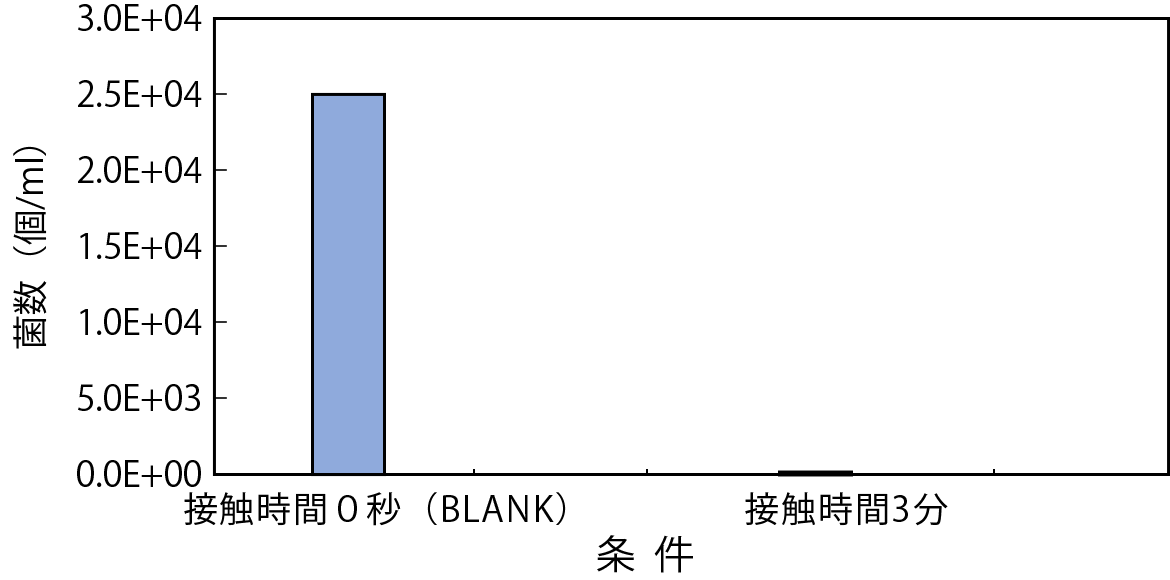
図-6 セレウス菌殺菌試験
5.考察
- 大腸菌、黄色ブドウ球菌、サルモネラ菌、腸炎ビブリオ菌、緑膿菌、セレウス菌においては、今回の条件下では10の4~6乗オーダーで100%に近い殺菌効果があると考えられる。
殺菌試験結果 写真(大腸菌)

大腸菌
ブランク n=1
大腸菌
ブランク n=2
大腸菌
ブランク n=3
大腸菌
微酸性電解水接触後 n=1
大腸菌
微酸性電解水接触後 n=2

大腸菌
微酸性電解水接触後 n=3
殺菌試験結果 写真(黄色ブドウ球菌)

黄色ブドウ球菌
ブランク n=1
黄色ブドウ球菌
ブランク n=2
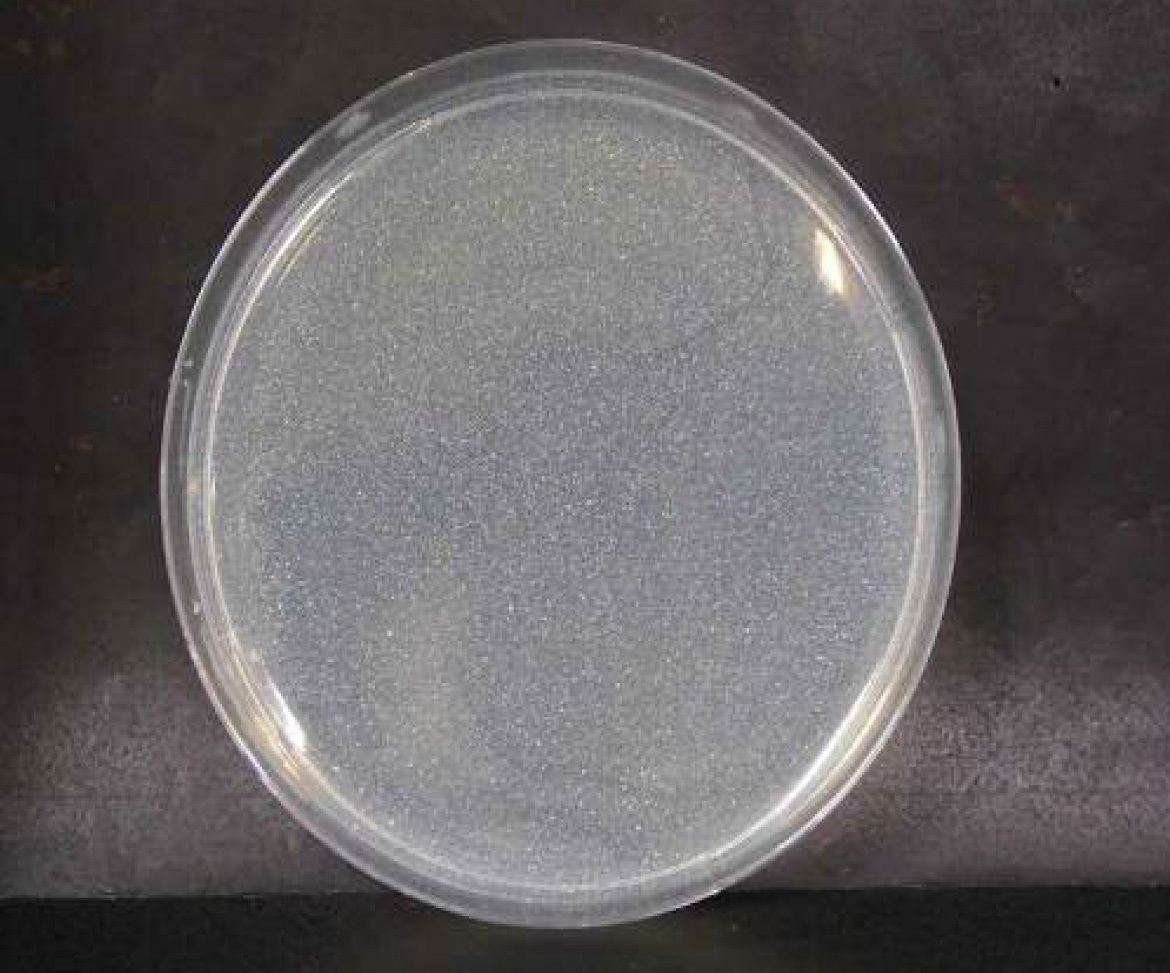
黄色ブドウ球菌
ブランク n=3
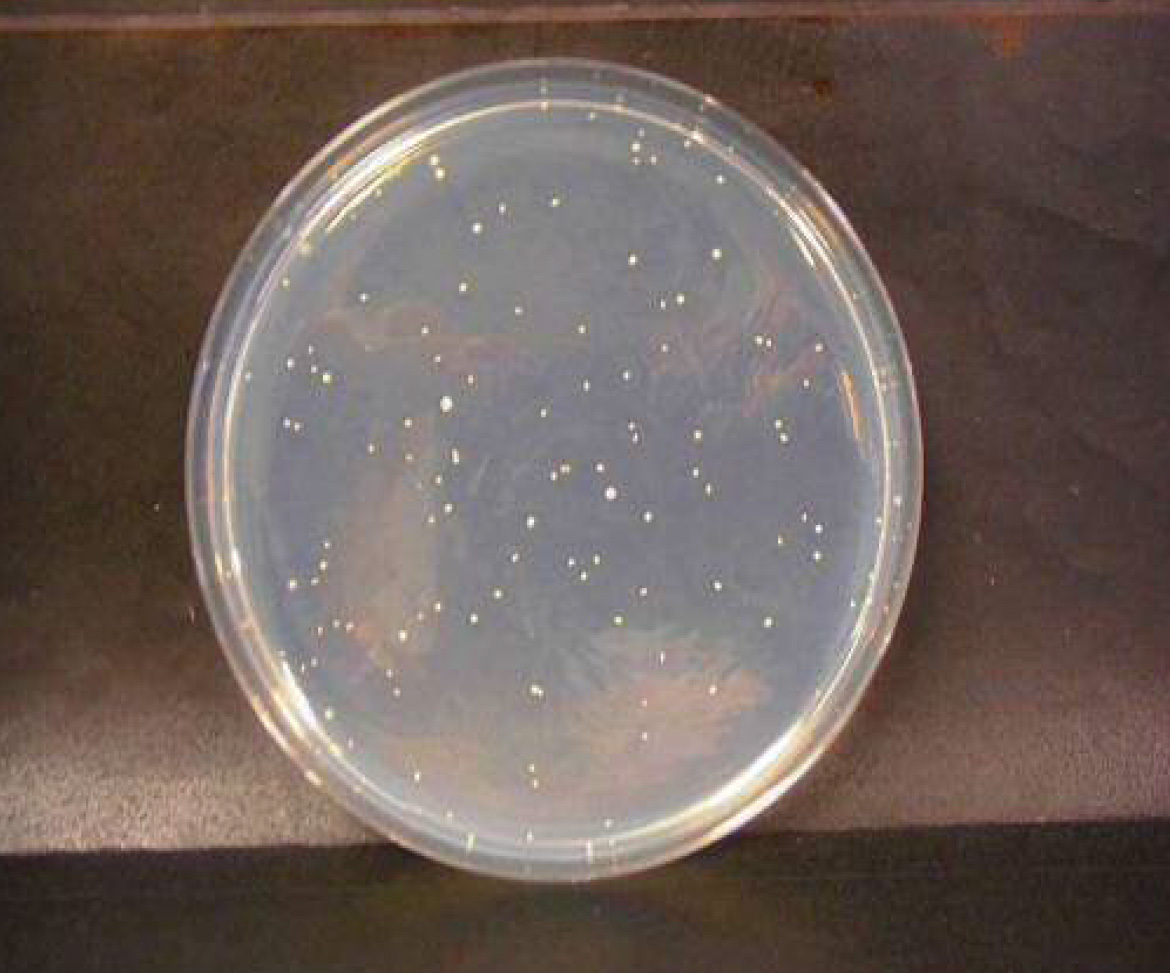
黄色ブドウ球菌
微酸性電解水接触後 n=1
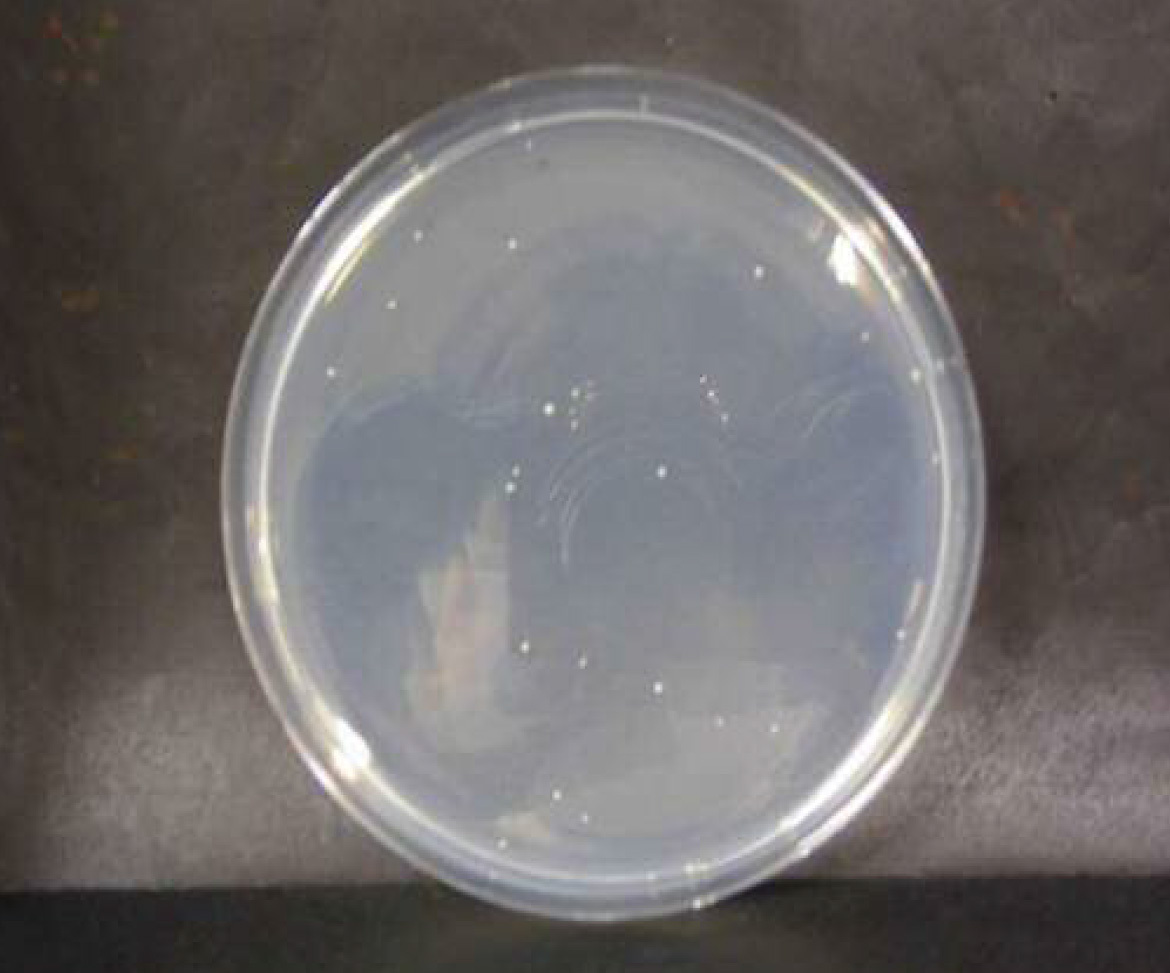
黄色ブドウ球菌
微酸性電解水接触後 n=2
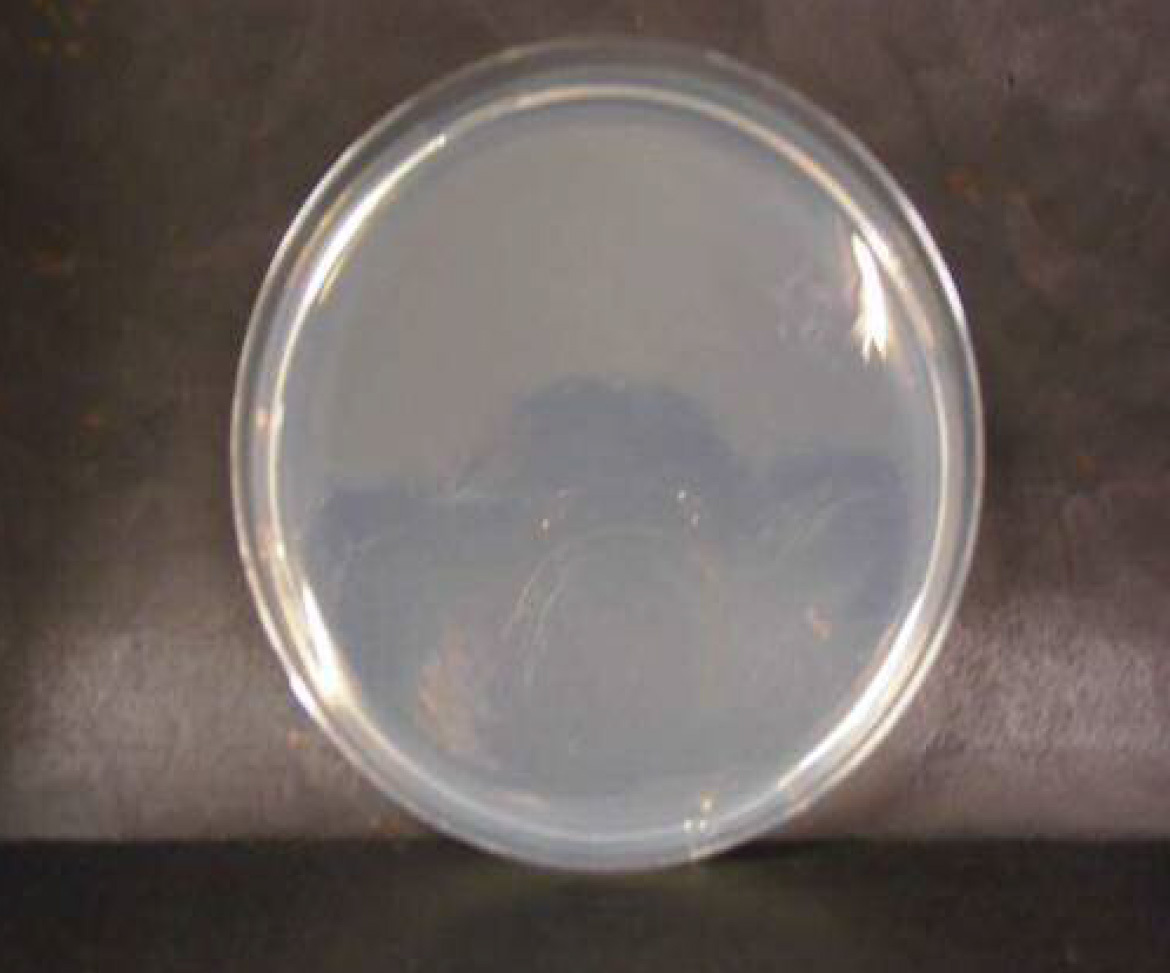
黄色ブドウ球菌
微酸性電解水接触後 n=3
殺菌試験結果 写真(サルモネラ菌)

サルモネラ菌
ブランク n=1
サルモネラ菌
ブランク n=2
サルモネラ菌
ブランク n=3
サルモネラ菌
微酸性電解水接触後 n=1

サルモネラ菌
微酸性電解水接触後 n=2
サルモネラ菌
微酸性電解水接触後 n=3
殺菌試験結果 写真(腸炎ビブリオ菌)
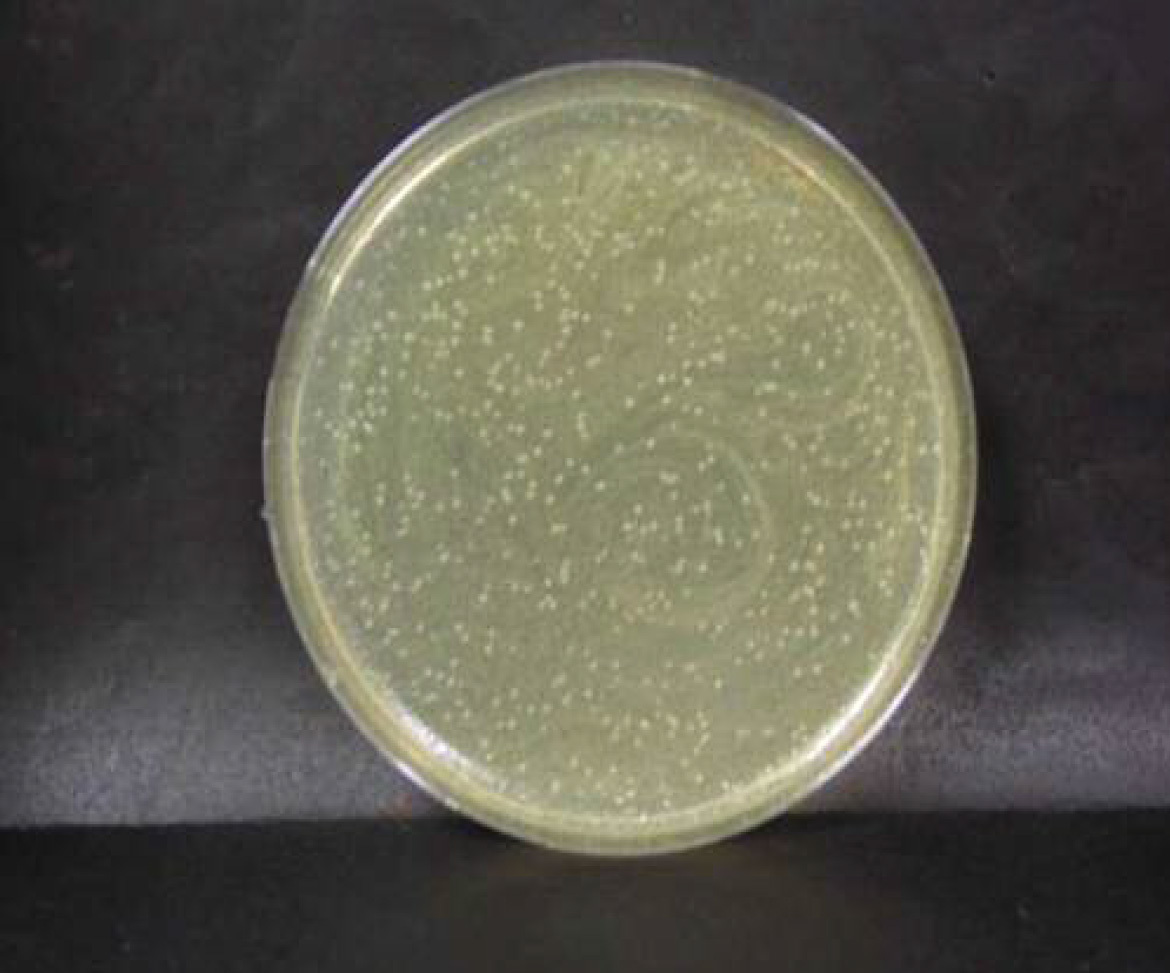
腸炎ビブリオ菌
ブランク n=1
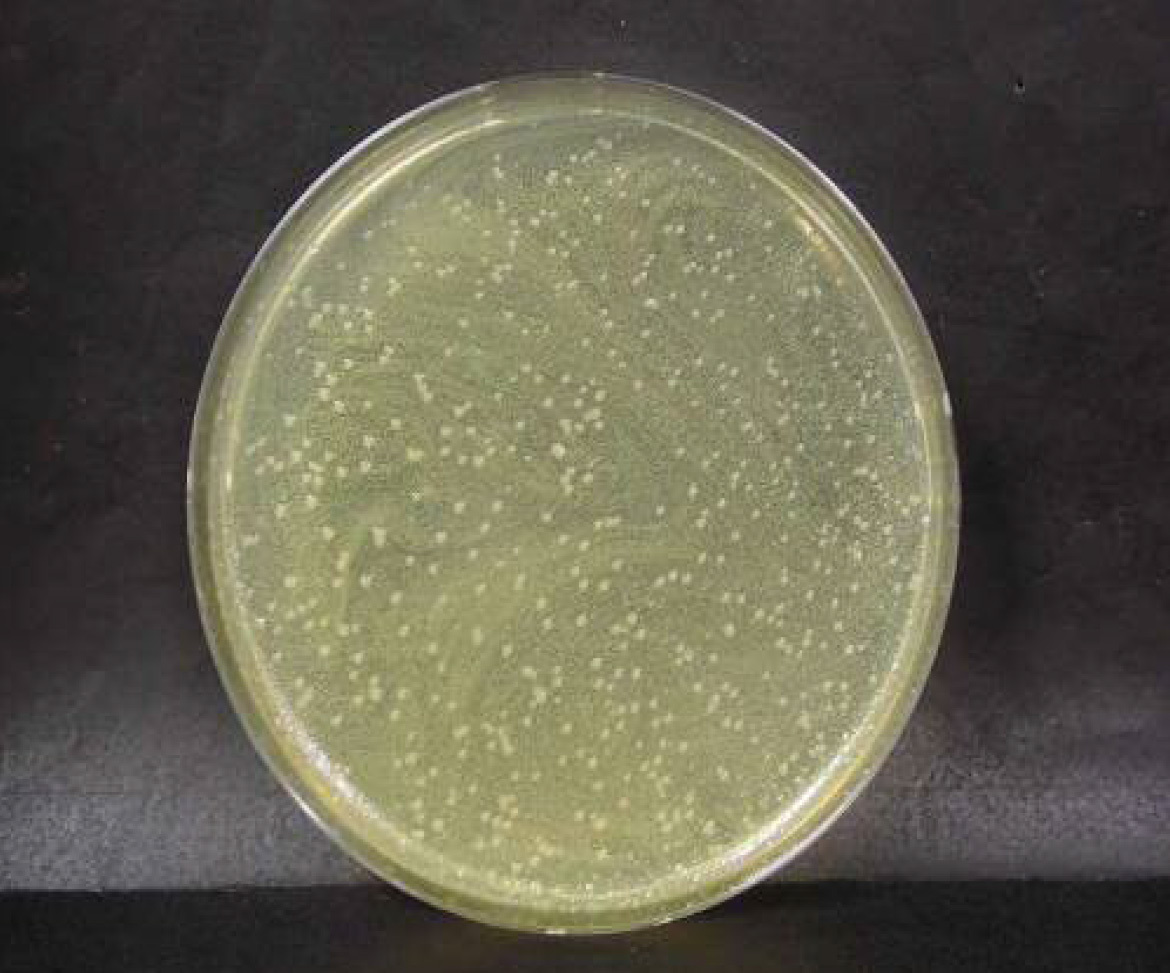
腸炎ビブリオ菌
ブランク n=2
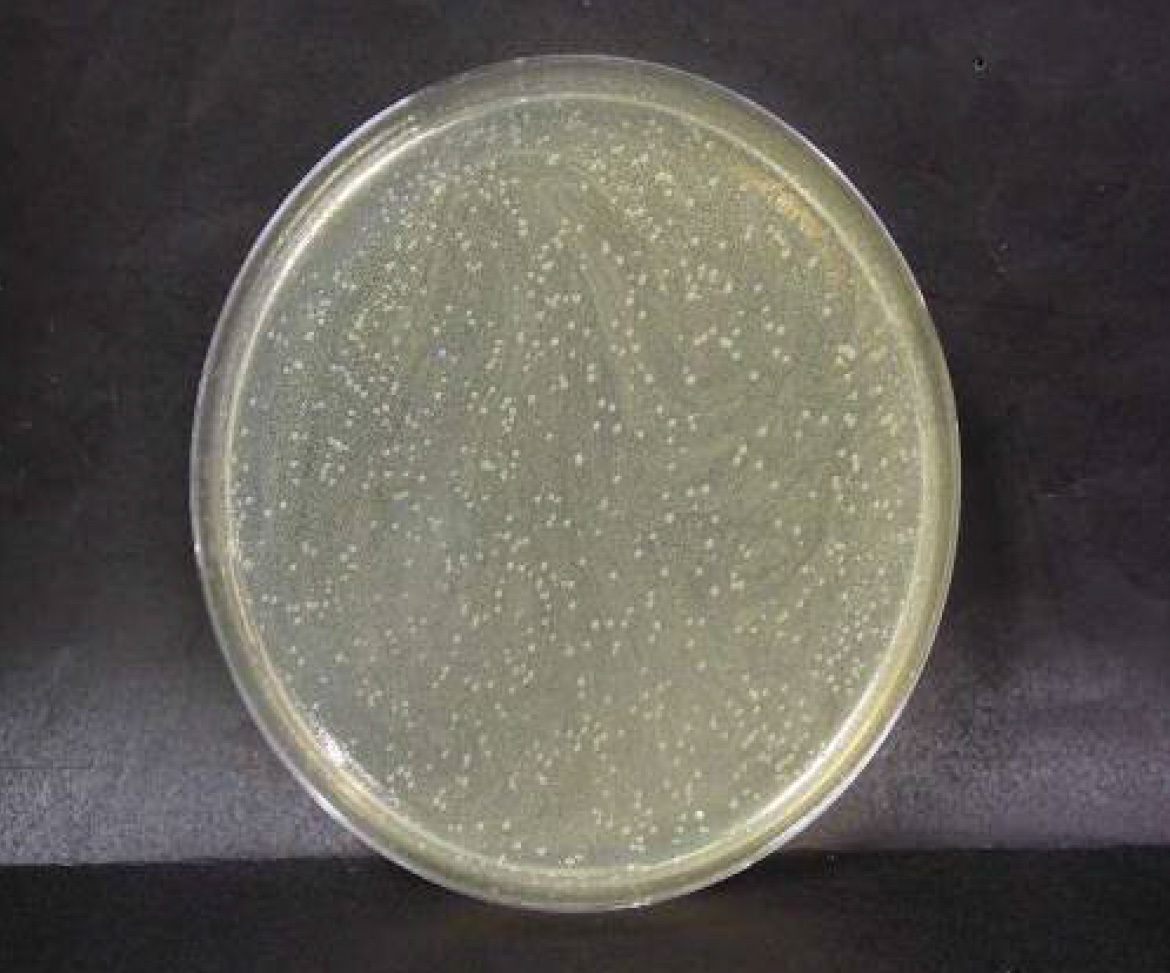
腸炎ビブリオ菌
ブランク n=3
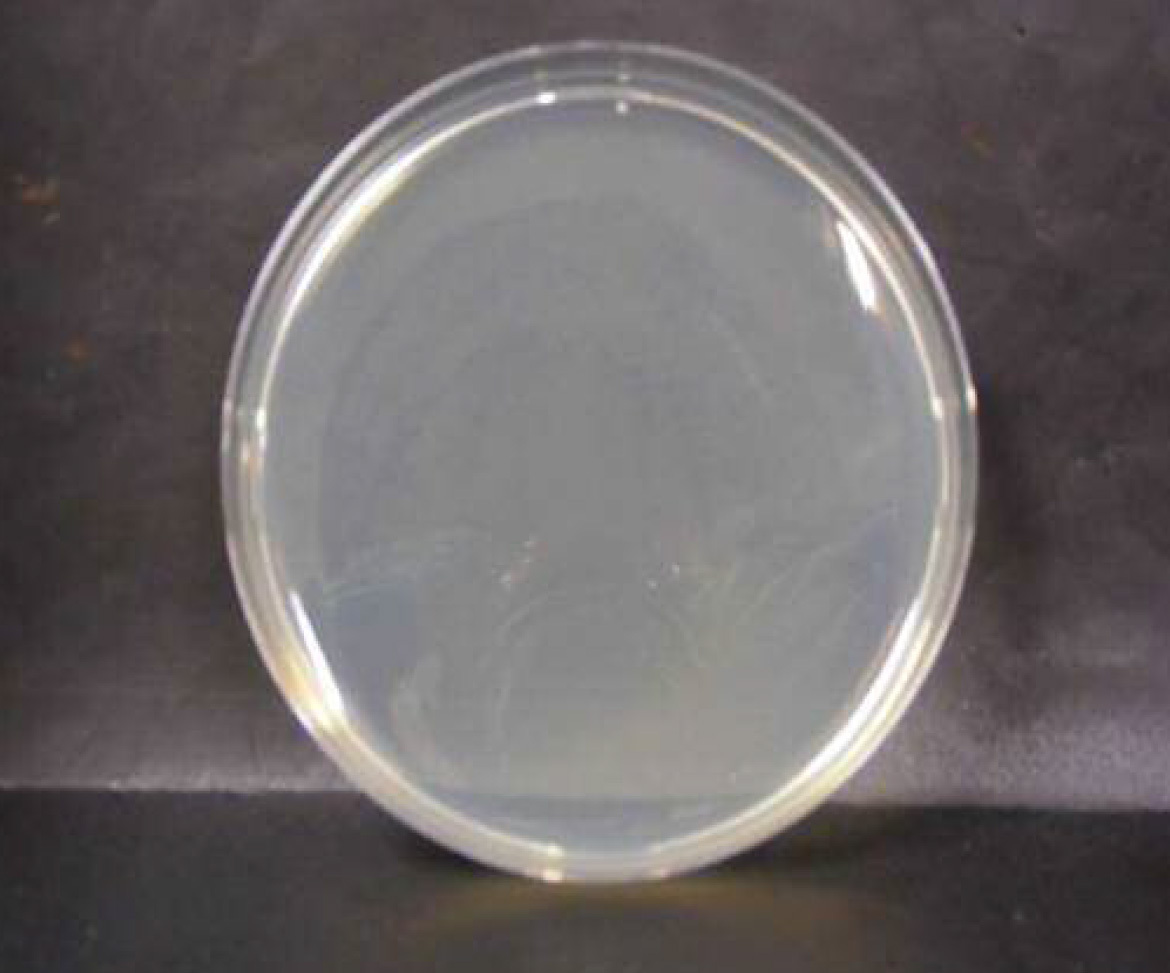
腸炎ビブリオ菌
微酸性電解水接触後 n=1

腸炎ビブリオ菌
微酸性電解水接触後 n=2
腸炎ビブリオ菌
微酸性電解水接触後 n=3
殺菌試験結果 写真(緑膿菌)
緑膿菌
ブランク n=1

緑膿菌
ブランク n=2
緑膿菌
ブランク n=3
緑膿菌
微酸性電解水接触後 n=1
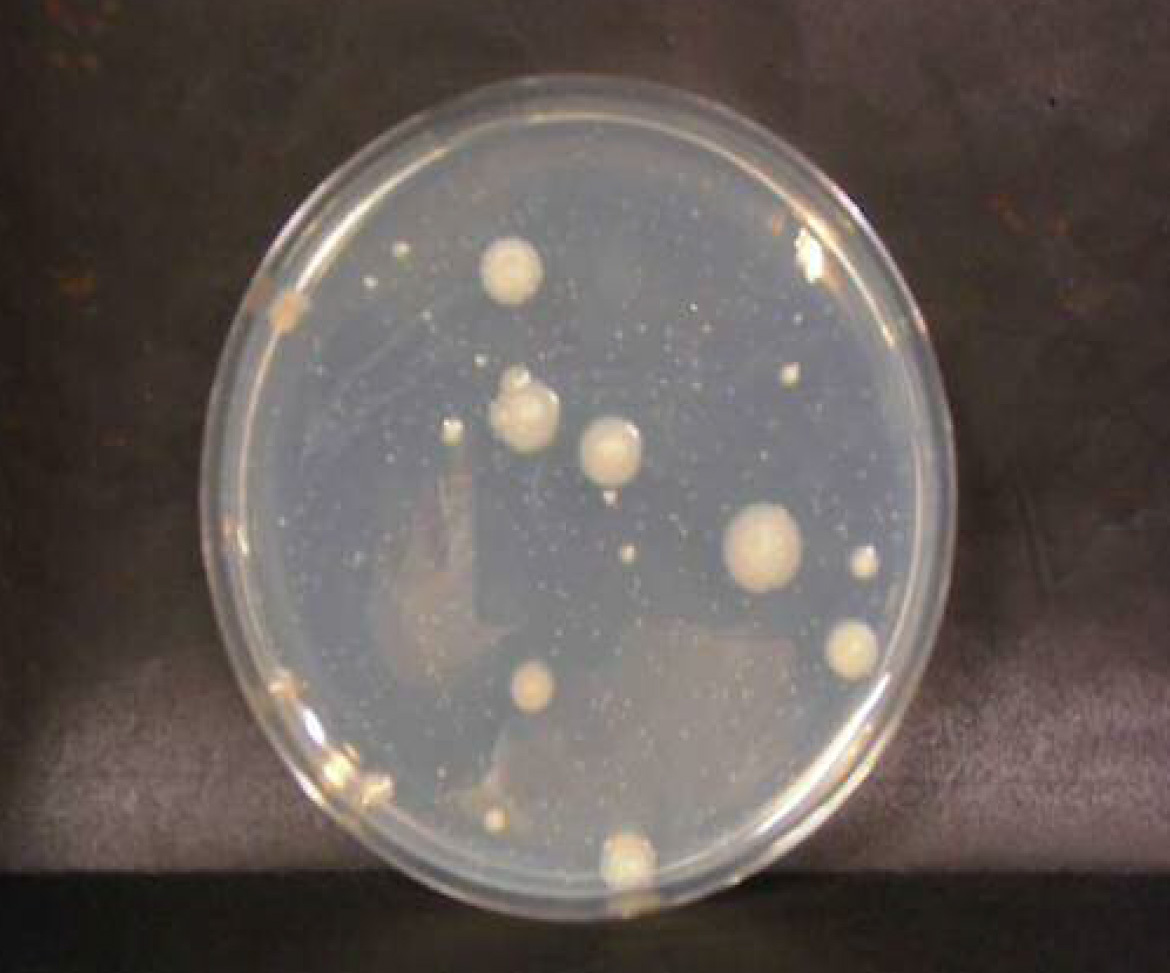
緑膿菌
微酸性電解水接触後 n=2
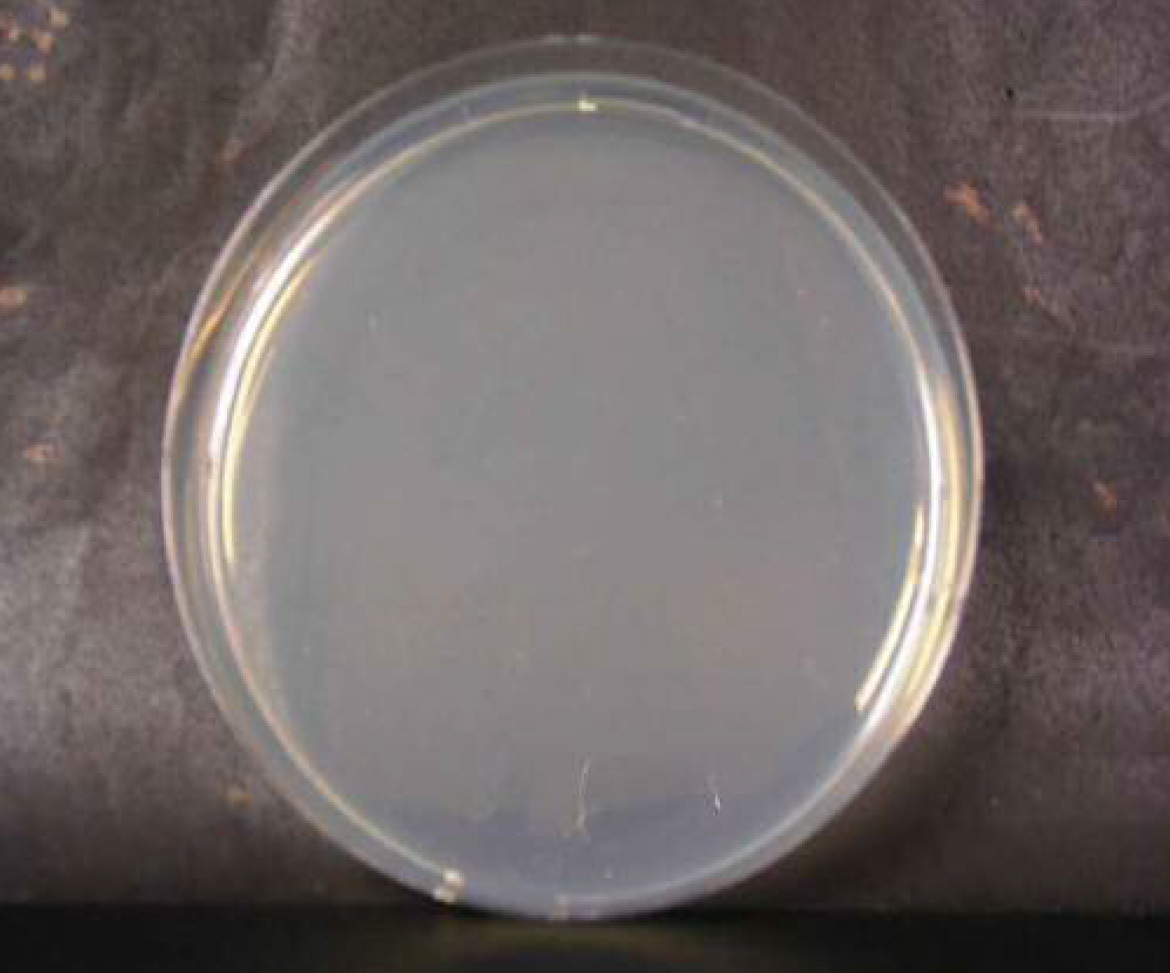
緑膿菌
微酸性電解水接触後 n=3
殺菌試験結果 写真(セレウス菌)
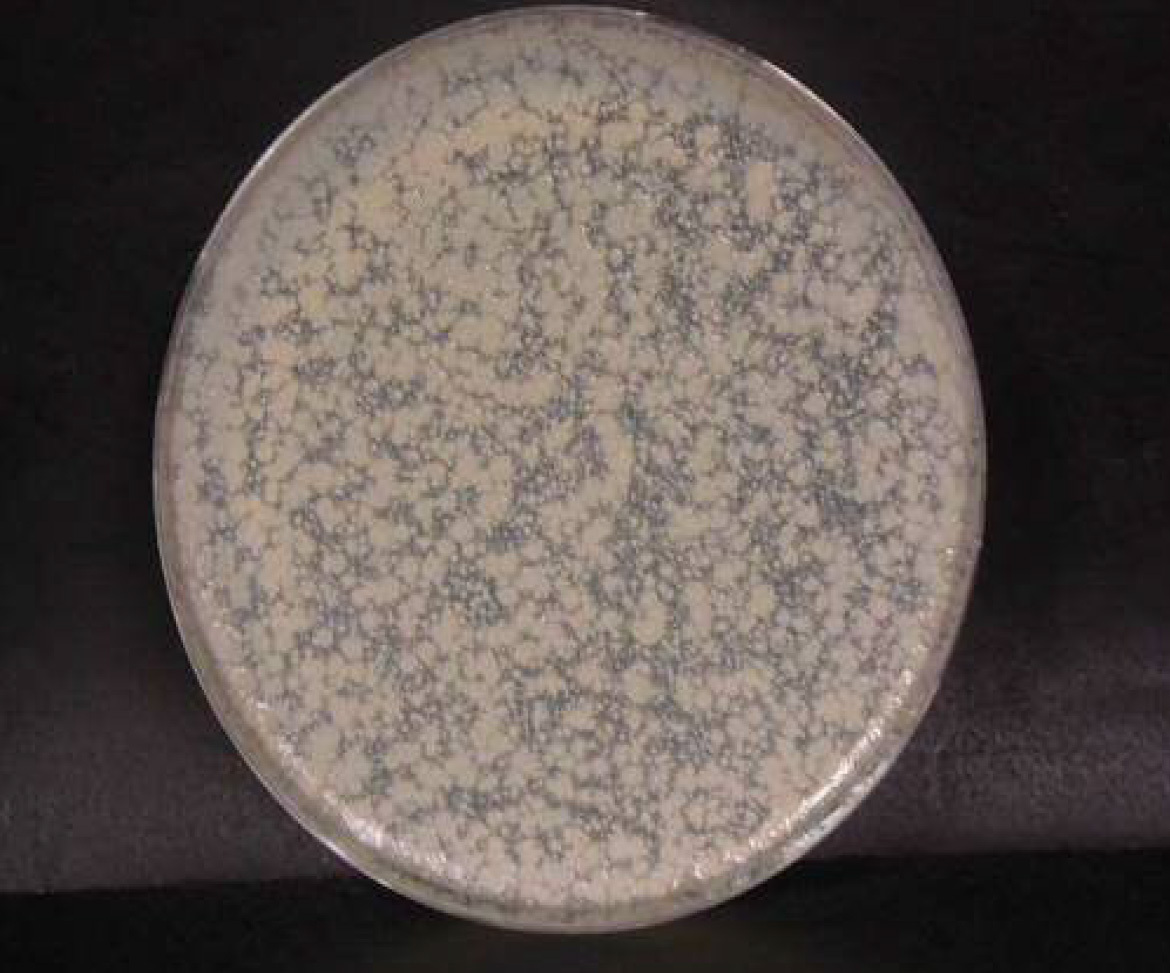
セレウス菌
ブランク n=1

セレウス菌
ブランク n=2

セレウス菌
ブランク n=3
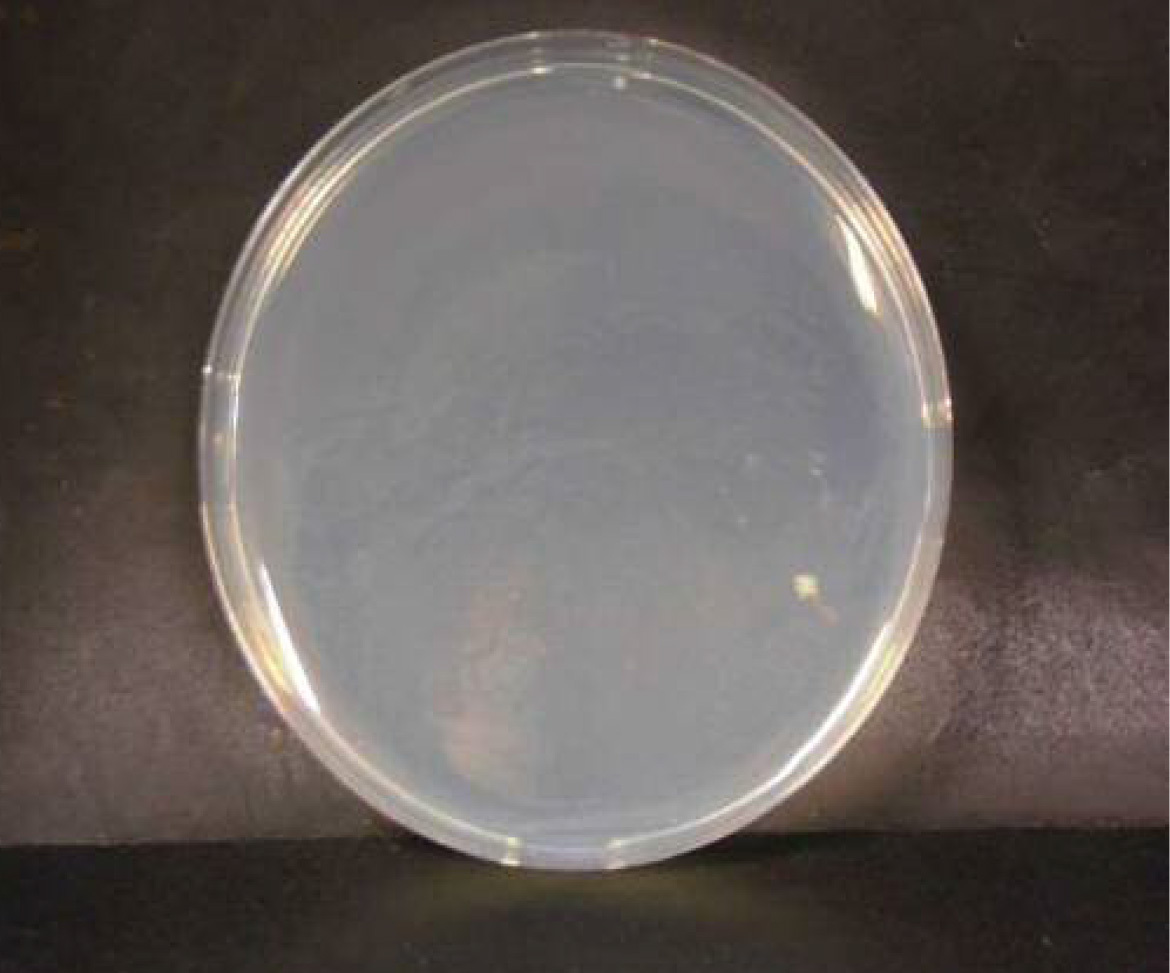
セレウス菌
微酸性電解水接触後 n=1
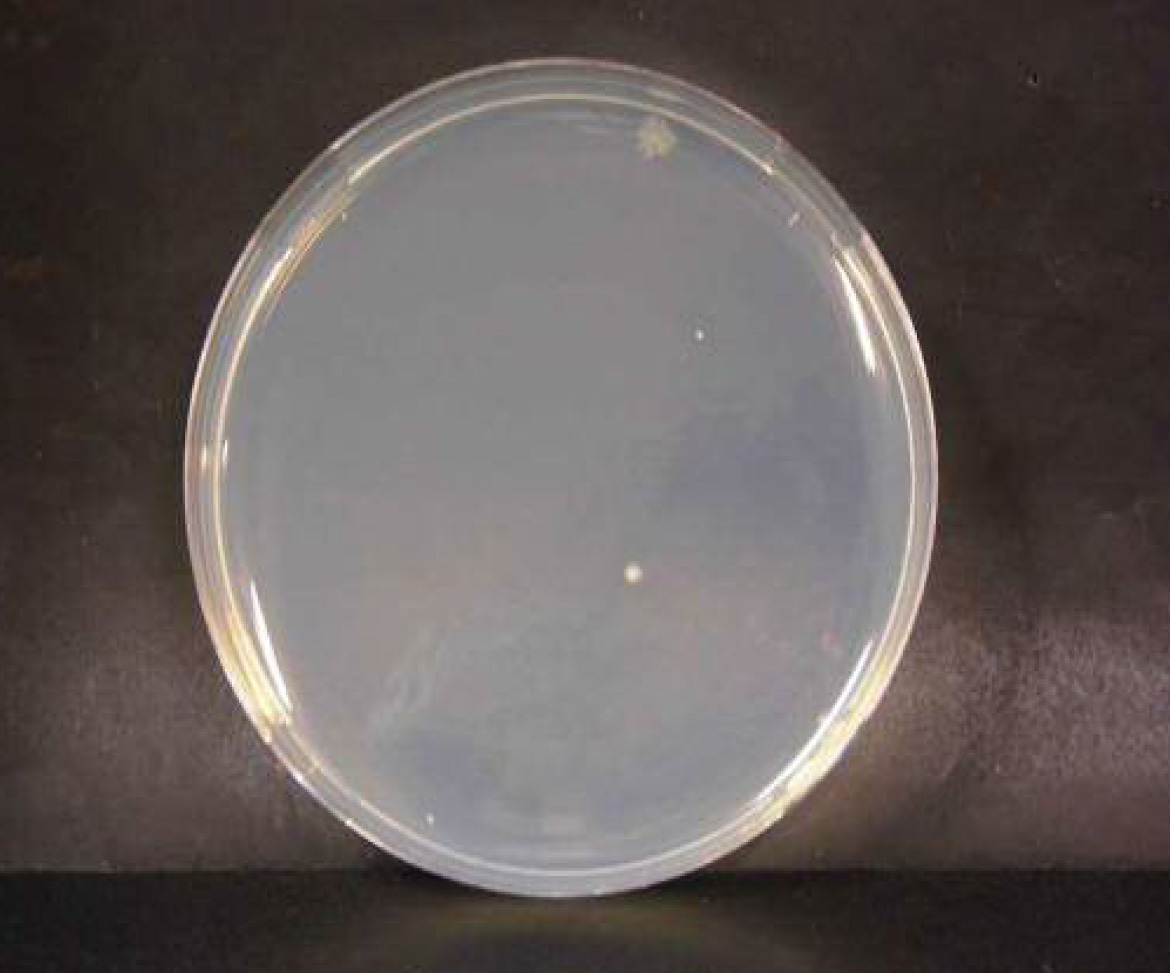
セレウス菌
微酸性電解水接触後 n=2
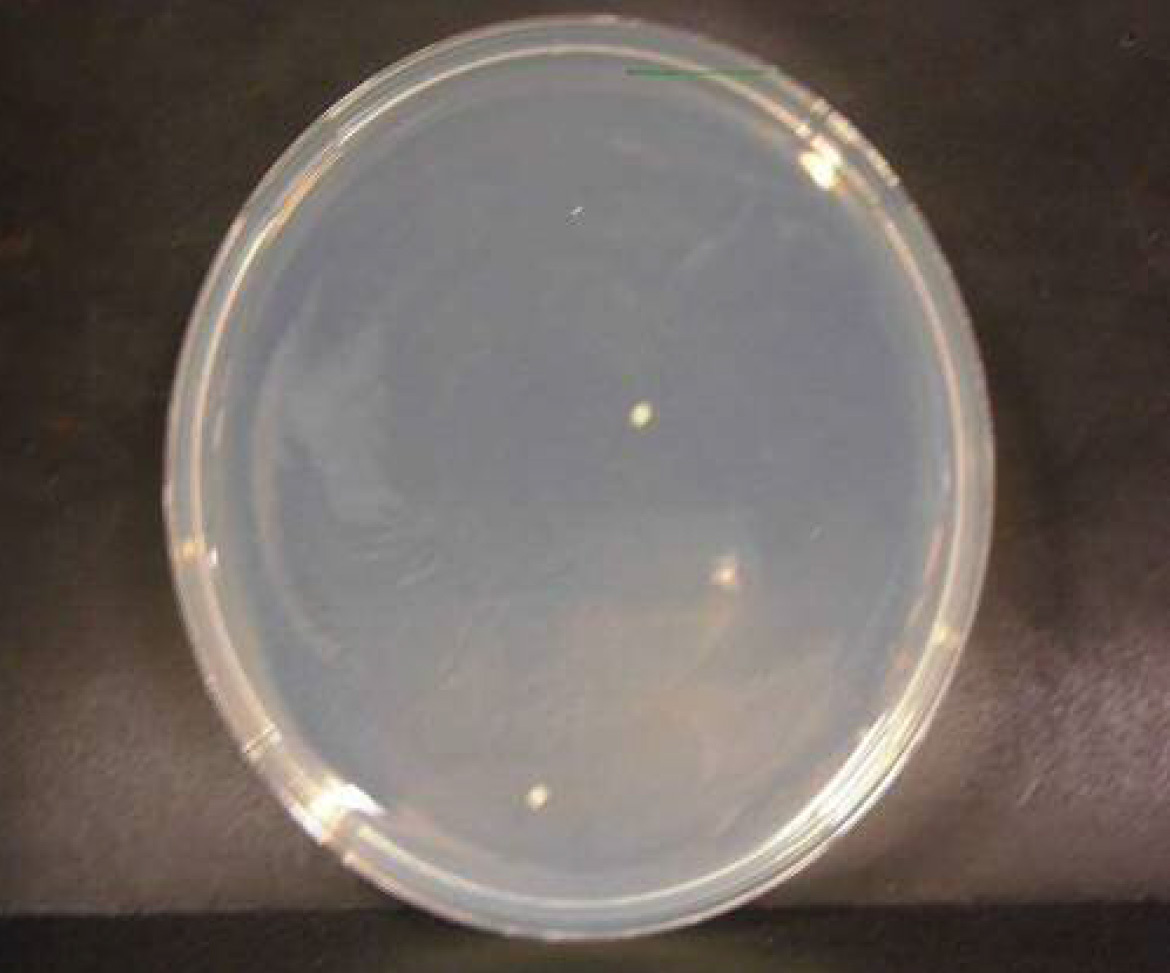
セレウス菌
微酸性電解水接触後 n=3
2.微酸性電解水「ジアセントⓇ」安定性試験結果
2021年11月18日(一般財団法人 鹿児島県環境技術協会)
1.目的
微酸性電解水(ジアセントⓇ)について保存期間中における成分変化を調査することを目的とした。
2.供試試料
製造元:富山薬品工業株式会社
製造日:令和3年3月16日
3.試験条件
20℃に設定したインキュベーター内に静置し、定期的に必要な量を採取し分析に供した。
また、未開封品として富山薬品工業株式会社内において常温保存および低温保存した試料について令和3年10月14日に開封し、同様に分析を行った。
4.試験期間
令和3年3月17日~令和3年10月6日
5.分析項目
| 項目 | 製品規格値 |
| pH | 5.0~6.5 |
| 有効塩素 | 20~40mg/kg |
6.試験結果
保存試験の結果を表1および図1に示す。
pHは試験開始後約2か月後に最も高い値を示し、その後緩やかに減少する傾向がみられた。有効塩素は試験開始から緩やかに減少する傾向がみられた。いずれの項目も29週間後の10月6日には製品規格値を下回っており、25週間後までは製品規格値を維持していた。
未開封品の分析結果を表2に示す。
未開封状態ではpHおよび有効塩素のいずれも低温状態で約6カ月後も製品規格値を維持していた。
表1 保存期間中におけるpHおよび有効塩素の変化
| 調査日 | pH | 有効塩素(mg/kg) |
|---|---|---|
| 3/17 | 5.1 | 24.8 |
| 3/24 | 5.1 | 24.4 |
| 3/31 | 5.1 | 24.0 |
| 4/7 | 5.2 | 23.8 |
| 4/14 | 5.3 | 23.6 |
| 4/21 | 5.4 | 23.7 |
| 4/28 | 5.4 | 23.6 |
| 5/6 | 5.5 | 23.3 |
| 5/12 | 5.5 | 23.5 |
| 調査日 | pH | 有効塩素(mg/kg) |
|---|---|---|
| 5/19 | 5.7 | 23.3 |
| 5/26 | 5.5 | 23.2 |
| 6/2 | 5.4 | 22.7 |
| 6/9 | 5.5 | 22.5 |
| 6/16 | 5.4 | 22.5 |
| 7/14 | 5.3 | 21.7 |
| 8/11 | 5.1 | 21.2 |
| 9/8 | 5.0 | 20.5 |
| 10/6 | 4.9 | 19.8 |
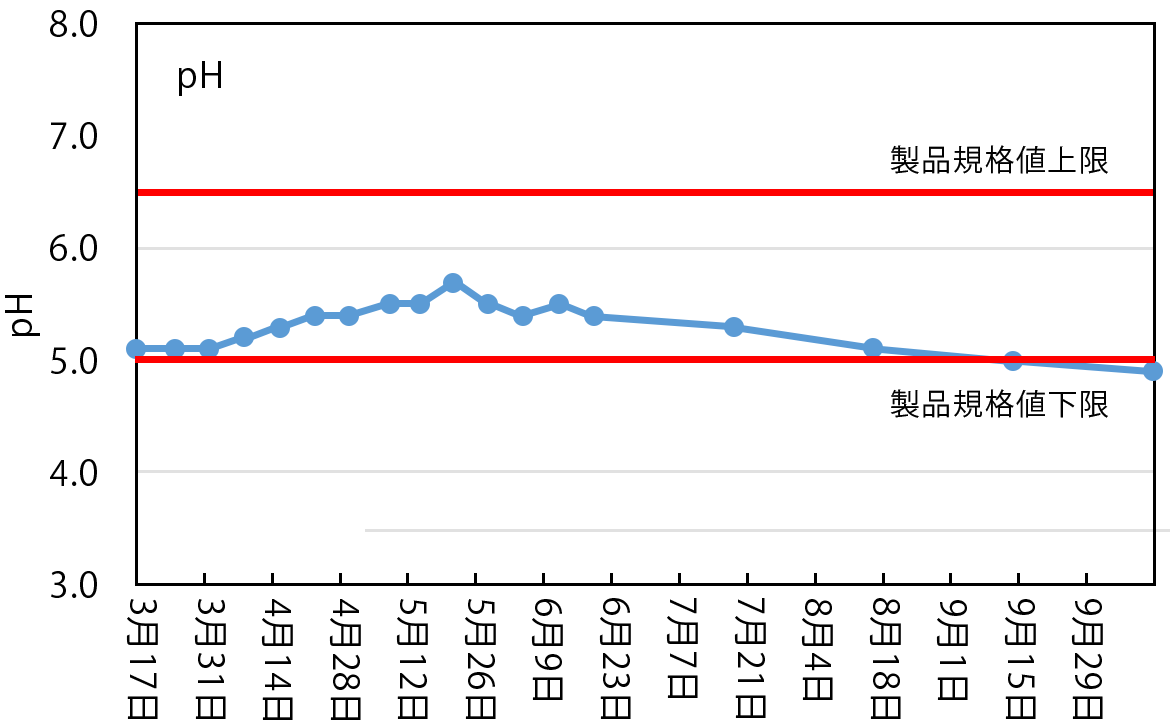
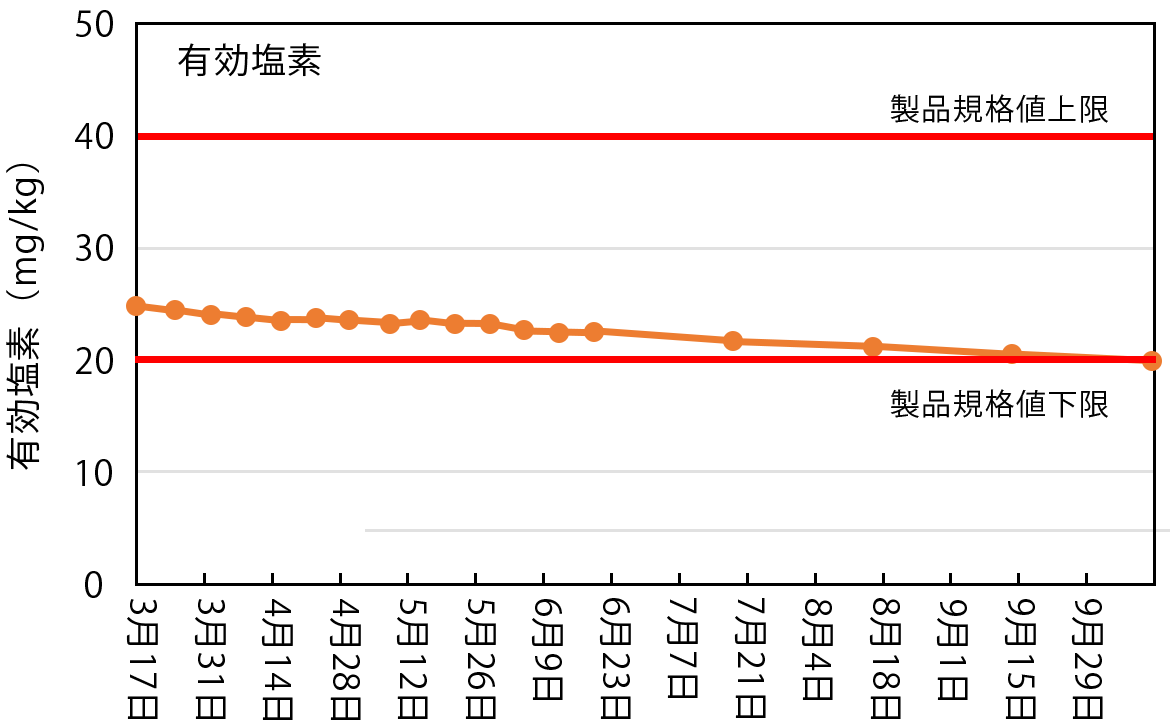
図1 保存期間中におけるpHおよび有効塩素の変化


